科发投后 | 晨伫科技公布乳腺癌PROTAC管线首批活性和动物实验数据
近日,科发资本投资项目晨伫科技研发团队公布了乳腺癌PROTAC管线首批活性和动物实验数据,基于晨伫MechGen多维度智能技术平台设计所获得的研究结果初步表明,所设计的靶向降解ER的PROTAC蛋白降解剂分子CZ-501,无论是在有效性还是安全性方面,均具有优异表现,活性等指标达到业内最好水平。
近日,科发资本投资项目晨伫科技研发团队公布了乳腺癌PROTAC管线首批活性和动物实验数据,基于晨伫MechGen多维度智能技术平台设计所获得的研究结果初步表明,所设计的靶向降解ER的PROTAC蛋白降解剂分子CZ-501,无论是在有效性还是安全性方面,均具有优异表现,活性等指标达到业内最好水平。
实验结果
有效性数据
实验数据表明,与同赛道Arvinas公司开发的临床Ⅲ期药物的ARV-471相比,CZ-501在MCF-7癌细胞中具有较高的靶标降解效率,达到世界领先水平,下图是两款PROTAC蛋白降解剂的靶标降解效率对比图。

研究还表明,除MCF-7癌细胞系外,CZ-501还可在其它多种乳腺癌细胞系(CAMA-1、MDA-MB-134-VI、T47D)中实现靶标蛋白降解效果,所表现出的优秀药效证实其具有较好广谱性。

安全性数据
1.药代动力学实验
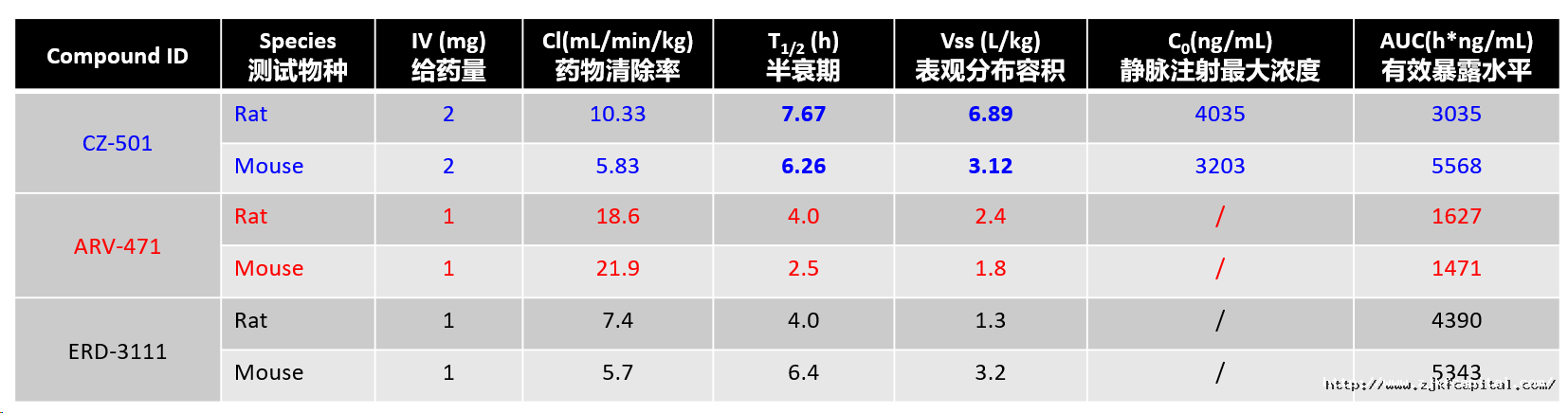
晨伫研发团队开展了半衰期、体内分布吸收、口服利用度等系列实验,同时与ARV-471、ERD-3111等在研药物公开数据进行了对比分析,结果表明:
(1)CZ-501具有适度药物清除率和较长半衰期,证明能够在生物体内较稳定存在,保证药物发挥时间;
(2)表观分布容积较大,说明CZ-501能够在体内广泛分布,可能具有良好的亲脂性,容易穿透细胞膜被癌细胞吸收;
(3)适度的AUC值反映出CZ-501在体内的稳定存在,与半衰期数据一致,同时又尽可能地避免了长时间暴露带来的药物毒性问题;
(4)口服利用度(F<10%)表明CZ-501更适用于静脉注射给药方式(与PROTAC主流一致)。
数据来源:J. Med. Chem. 2023, 66, 17, 12559–12585
2.毒理学实验
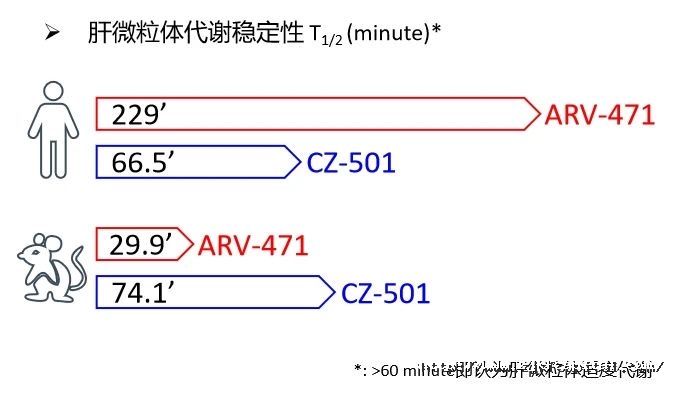
肝微粒体代谢实验数据表明,CZ-501在肝微粒体中适度代谢,既保证一定稳定性能发挥药效,又避免药物累积带来的潜在毒性。
心脏毒性等毒理学实验数据表明,CZ-501对P450酶、hERG酶都不具有抑制作用,具有优秀的药物安全性。

目前公司正在进一步扩大样本量和实验范围,加快推进体内外动物安全性和有效性实验进程,预计于2025年上半年进入IND申报阶段。
关于PROTAC
蛋白水解靶向嵌合体(Proteolysis targeting chimera,PROTAC)技术是一种新兴的靶向蛋白降解技术,该技术突破性的利用细胞自身的降解系统清除致病蛋白,为蛋白质降解研究开辟了新的途径,是药物设计中非常有前途的研究策略。
PROTAC的概念最初于2001年由Sakamoto和Crews首次提出,他们设计了第一个基于肽的PROTAC分子,命名为PROTAC-1,用于降解蛋氨酸氨基肽酶2 (METAP2)。PROTAC通过利用泛素-蛋白酶体系统选择性诱导蛋白质降解。在结构上,它由三个部分组成:连接结合靶蛋白的配体、连接体和连接E3连接酶的配体。经过20多年的发展,至今已有越来越多针对各种蛋白的PROTAC被广泛报道,特别是一些针对恶性肿瘤的PROTAC已被开发出来作为临床试验候选药物。
新型PROTAC降解剂兼具抗癌潜力、良好的药物性能,还可有效解决传统疗法无法解决的难以靶向目标蛋白以及耐药性等问题。据不完全统计,截至2022年底,全球至少有20余种PROTAC项目进入临床试验。已进入临床阶段的Bavdegalutamide、ARV-471和NX-2127等药物已证实了PROTAC用于癌症治疗的活性和未来应用潜力。PROTAC技术可应用的靶点广泛,临床应用前景广阔,随着技术的不断成熟、发展和应用,未来将使更多患者受益。
晨伫研发平台
晨伫MechGen多维度智能研发技术平台,采用最前沿诺奖级技术,深度研究靶标蛋白机理、药物分子虚拟筛选、新型人工智能药物设计优化方法等药物发现全流程技术,具备快速获得优质先导化合物的技术实力。其中,CZ-501就是公司基于该平台获得的最重要成果之一。
平台包括高性能·靶标蛋白机理研究平台、高通量·药物分子虚拟筛选平台、高智能·人工智能药物设计平台、高水平·药物分子设计优化平台、高规模·药物分子碎片数据库平台、高效率·多管线药物研发平台,涵盖药物设计全流程,提供全方位的一站式综合技术服务。
项目背景
乳腺癌是一种最常见的发生在乳腺上皮组织中的恶性肿瘤, 其致死率位居女性恶性肿瘤首位。内分泌治疗抑制雌激素是激素受体阳性乳腺癌治疗首选策略。然而,芳香化酶抑制剂和选择性雌激素受体调节剂等药物耐药问题是导致乳腺癌临床治疗失败的主要原因之一,这也是目前临床亟需解决的挑战性问题。
雌激素受体(Estrogen Receptor, ER)是类固醇激素受体,也是一种雌激素调节转录因子,在乳腺癌的发生和增殖中起关键作用。据统计,近80%的乳腺癌与ER功能异常相关,ERα是乳腺癌内分泌治疗的一个重要靶点。通过蛋白酶体途径降解ERα蛋白的PROTAC,已成为绝经后内分泌抵抗性乳腺癌或晚期转移性ERα阳性乳腺癌患者的主要治疗选择。
2023年10月,晨伫研发数据初步证实,团队所设计的靶向降解ER的PROTAC蛋白降解剂分子可以显著降低人乳腺癌MCF-7细胞内ERα蛋白水平,活性等数据达到赛道最好水平。






 浙公网安备33011302000656
浙公网安备33011302000656